
Cómo la IA puede ayudar a los pacientes con cáncer a recibir un tratamiento personalizado y preciso más rápido
Por: Catherine Bolgar.
Durante una visita clínica típica de 15 a 20 minutos con los pacientes, el oncólogo Dr. Rom Leidner abre alrededor de 20 archivos diferentes en su computadora. Son piezas de un rompecabezas que crea una imagen del cáncer del paciente: resultados de análisis de sangre, tendencias de peso, imágenes radiológicas, microbiología, patología, cardiología, mensajes electrónicos de otros médicos, mensajes electrónicos de pacientes, páginas de texto de enfermeras y personal clínico, recetas, órdenes de quimioterapia, formularios de seguro.
Para algunos archivos, tiene que iniciar sesión en un software especializado para acceder. Y después de revisar todo eso, puede examinar al paciente y hablar sobre su atención oncológica. Para cumplir con su horario de atención a los pacientes, el Dr. Leidner y muchos médicos recurren a pasar los fines de semana en copiar y pegar toda esta información en las historias clínicas con anticipación.

«La última esperanza de nuestra profesión bien puede ser la curación asistida por IA de los flujos de información que convergen en la sala de examen», dice el Dr. Leidner, oncólogo médico especializado en hematología en la Clínica Franz del Instituto Oncológico de Providence en Portland, Oregón.
Providence, una organización de atención médica de 51 hospitales que atiende a siete estados occidentales de los EE. UU., trabaja para hacer justo eso, desarrollar prototipos de herramientas de IA de investigación para clasificar las crecientes montañas de datos de los pacientes, en el tiempo de vuelo, para mejorar las terapias y avanzar en el tratamiento del cáncer, que representa casi una de cada seis muertes en todo el mundo.
Las pruebas de laboratorio, las exploraciones y los análisis genéticos más refinados pueden ayudar a promover una mejor comprensión del caso de cada paciente, lo que resulta en terapias personalizadas que adaptan el tratamiento y la medicación a los biomarcadores genéticos de cada paciente. Evaluar toda esa información es una tarea enorme.
«Es una convergencia afortunada en los últimos dos años, que justo cuando nos acercamos a un cuello de botella con datos celulares y moleculares hiperplexados de ensayos clínicos que excederán la capacidad humana para analizarlos con facilidad, parece que estamos a las puertas de una tecnología transformadora capaz de manejar los flujos de datos que prevemos en la ciencia médica de próxima generación. «, dice el Dr. Leidner.
Providence trabaja con Microsoft en prototipos de herramientas de IA para mejorar la atención a los pacientes con cáncer, acelerar el progreso en la comprensión del cáncer y tal vez encontrar tratamientos o curas. El proyecto forma parte del compromiso de Microsoft de aplicar la IA generativa a la salud de precisión.

«Nuestra colaboración de investigación en Providence ha comenzado a dar sus frutos en aplicaciones integrales del mundo real hacia la medicina de precisión. Los avances tecnológicos subyacentes pueden capacitar a los profesionales clínicos e investigadores para desbloquear cada vez más aplicaciones de alto valor para mejorar la atención al paciente y acelerar el descubrimiento biomédico», dice Hoifung Poon, Ph.D., gerente general de Health Futures en Microsoft Research, quien ha colaborado con Providence en estos prototipos de herramientas de IA.
La información del paciente existe en una variedad de formatos: registros médicos electrónicos (EMR, por sus siglas en inglés), escaneos de imágenes, genómica y todo tipo de pruebas de laboratorio. La misma información puede anotarse a través de la utilización de diferentes términos o diferentes formatos y la información central requiere sintetizar una gran cantidad de datos no estructurados. Este es justo el tipo de trabajo que la IA puede hacer bien: resumir datos no estructurados en forma de texto.
Para los pacientes con cáncer que han agotado la primera línea de tratamientos, un ensayo clínico, en el que se prueban nuevos tratamientos, puede ofrecer la mejor última esperanza. Lo difícil es encontrar uno. El porcentaje de pacientes con cáncer en los Estados Unidos que participan en un ensayo es de un solo dígito, sin embargo, irónicamente, la falta de inscripción es una razón clave por la que los ensayos clínicos fracasan.
Este problema no tiene nada que ver con la escasez de ensayos clínicos. De hecho, el número de ensayos clínicos registrados (para todos los tratamientos, a nivel mundial), se multiplicó por 59 entre 2000 y 2021, según la Organización Mundial de la Salud. En Estados Unidos, el número de estudios registrados se multiplicó por 289 en ese mismo período.
En cambio, uno de los mayores obstáculos para la inscripción en ensayos clínicos son los datos. Una vez más, el problema no es la escasez, sino todo lo contrario: montañas de registros.
«El estado funcional de un paciente, la ubicación del cáncer, los recuentos sanguíneos, la función de órganos críticos como el corazón, el hígado y los riñones, y muchos otros criterios deben evaluarse de manera cuidadosa para cada paciente potencial, en cada estudio clínico», dice el Dr. Leidner, quien dirige un ensayo clínico de terapia adoptiva de células T transducidas por TCR modificadas a nivel genético dirigida al neoantígeno KRAS. Se trata de un tipo de inmunoterapia en la que las propias células T de un paciente se diseñan para reconocer y erradicar de manera específica las células cancerosas con mutaciones en el gen KRAS asociadas con el cáncer.
Como si las piezas del rompecabezas médico no fueran lo suficientemente difíciles como para encajar, es posible que también falte información logística básica en los registros de los pacientes. «Puede ser sorprendente, pero identificar al oncólogo de un paciente u otros especialistas que han estado involucrados no es necesariamente sencillo. Este tipo de información debería organizarse de manera sencilla en el registro del paciente, pero en realidad a menudo está fragmentada o ausente», dice el Dr. Leidner.
Donde brilla la IA
El desafío no es solo la multiplicidad de variedades de información para cada paciente, sino también la fragmentación de los formatos de EMR de una clínica o sistema de salud a otro. La IA, sin embargo, puede resumir esta información de manera rápida. Y lo que es más importante, no requiere que la información esté formateada: puede aspirar los resultados de laboratorio, las notas de los médicos y los escaneos digitalizados tal como están. También puede darse cuenta de que dos términos diferentes se refieren a lo mismo, porque puede funcionar con lenguaje natural.
«La IA es muy útil para revisar las bases de datos de los ensayos de investigación, recopilar múltiples criterios de elegibilidad de los ensayos y compararlos con cada paciente individual mediante la selección de esa información de la historia clínica digital», dice el Dr. Leidner. «Como médico, simplemente no hay suficientes horas en el día para examinar el proceso de emparejamiento de los ensayos y seguir viendo a los pacientes».
Una cosa que será menos importante en la investigación clínica es el sitio de origen del cáncer de un paciente o la categorización morfológica: «esto es algo bastante difícil de comprender incluso para la profesión médica», dice el Dr. Leidner. En algunos ensayos clínicos avanzados, «es más una cuestión de ‘¿tienen el sistema inmunitario correcto y la mutación genética correcta en lugar de qué tipo de cáncer?'».
Las pruebas genéticas de los cánceres ahora son rutinarias, pero la tipificación HLA (para el antígeno leucocitario humano, un conjunto de genes que regulan el sistema inmunitario), aunque es rutinaria para los trasplantes de órganos, aún no es común en oncología. Providence ha hecho que la tipificación de HLA sea estándar para los pacientes con cáncer para permitir la medicina personalizada y poder encontrar con rapidez ensayos que ofrezcan una posible coincidencia.

La medicina personalizada en oncología «se basa en la presencia o ausencia de alteraciones genómicas. Cada terapia es específica para esas alteraciones, y estas pueden ser muy raras», dice el Dr. Carlo Bifulco, director médico de Providence Genomics, una división de Providence que utiliza la IA para transformar la atención médica.
Piensen en todas estas piezas como píxeles en una fotografía. En una imagen de baja resolución, es posible adivinar qué tipo de ave está en una foto, pero con alta resolución, es más fácil reconocer la especie gracias a detalles específicos.
El tratamiento del cáncer por el órgano donde se produce, como el cáncer de pulmón, es una analogía de baja resolución. Al aumentar la resolución, queda claro que el cáncer de un paciente está impulsado por un conjunto de aberraciones genéticas y el de otro paciente está impulsado por un conjunto diferente: son diferentes a pesar de que ambos son cáncer de pulmón.
Los biomarcadores no son el final de la historia. Otros atributos, como la salud general, la tolerancia a los medicamentos contra el cáncer, la edad y otros problemas de salud del paciente agudizan aún más la resolución. Esta representación holística de alta resolución se denomina «integración del paciente». Para encontrar suficientes pacientes con una incorporación de pacientes similares para un nuevo tratamiento que se somete a un ensayo clínico, es necesario comenzar con un gran grupo de pacientes.

Los Institutos Nacionales de Salud (NIH, por sus siglas en inglés) mantienen una base de datos voluntaria de ensayos clínicos, «pero solo tiene una interfaz de búsqueda rudimentaria», dice Poon. Solo en los Estados Unidos, hay dos millones de nuevos pacientes con cáncer cada año. Mientras tanto, en un momento dado, hay miles de ensayos activos.
«El proceso manual actual es irremediablemente no escalable», añade. «Nuestro sueño es estructurar toda la información médica y crear una integración de pacientes de alta fidelidad para que coincida en automático con los ensayos de forma continua, para permitir así el emparejamiento de ensayos clínicos justo a tiempo y democratizar esta fuente tan importante de atención médica de alta calidad. Como equipo de investigación, ha sido emocionante trabajar con Providence. El desarrollo de prototipos de herramientas de IA que utilicen los principios de la IA responsable, como la equidad, la privacidad y la seguridad, y la fiabilidad y la seguridad, es importante cuando buscamos mejorar los resultados de los pacientes en el futuro».
Con los últimos avances en IA generativa y el prometedor punto de prueba inicial en Providence, ya se puede imaginar la creación de un panel de control a escala poblacional para que los investigadores clínicos encuentren posibles candidatos a ensayos en tiempo real.
Si bien la IA desenreda la logística de la coincidencia de ensayos clínicos, podría tener un papel aún más importante en el descubrimiento médico. «Buscamos cada vez más y nuevas formas de comprender la biología del cáncer y, a través de eso, descubrir formas de erradicar el cáncer», dice el Dr. Leidner.
El objetivo es desarrollar modelos informáticos que puedan tomar las enormes cantidades de datos generados en los ensayos clínicos y los datos del mundo real para detectar una tendencia y luego demostrar que la terapia causó la tendencia. «Hoy en día, a partir de una biopsia, obtenemos gigabytes de datos a nivel celular y molecular», dice el Dr. Leidner. «Puede haber decenas de miles de variables en cada visita de un paciente en un ensayo clínico.
Estos conjuntos de datos simplemente están más allá de la capacidad humana para analizarlos. Dada la escala, es concebible que se requieran decenas de doctores, que trabajen durante años, para completar el análisis de un ensayo clínico».
La promesa del aprendizaje automático multimodal
Providence y Microsoft trabajan juntos en el aprendizaje automático multimodal, entrenado con diversos datos generados y gestionados por Providence: texto, imágenes o genómica y, en el futuro, biología espacial, proteómica (el estudio de las proteínas en nuestros cuerpos), transcriptómica (el estudio del ARN del cuerpo) y epigenómica (el estudio de la superestructura reguladora del genoma).
«Reunimos fuentes de datos muy complejas, que pueden ser imágenes, conjuntos de datos genómicos o solo texto, y hay flujos de datos gigantescos que pueden beneficiarse de este enfoque», dice el Dr. Bifulco. «La técnica ya ha comenzado a hacer coincidir las soluciones. Ya lo tenemos frente a oncólogos, enfermeras de investigación y patólogos, y lo usamos todos los días».
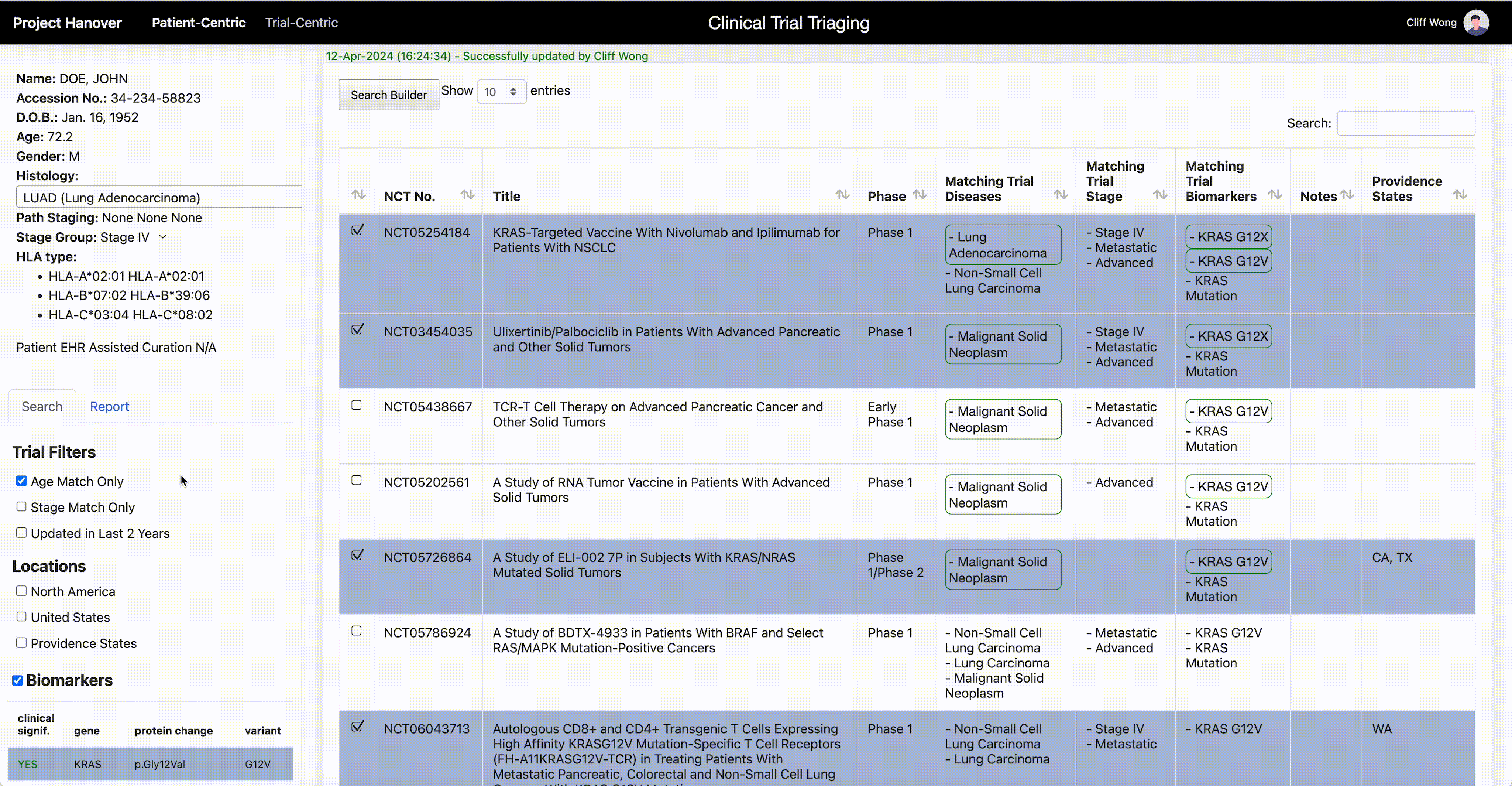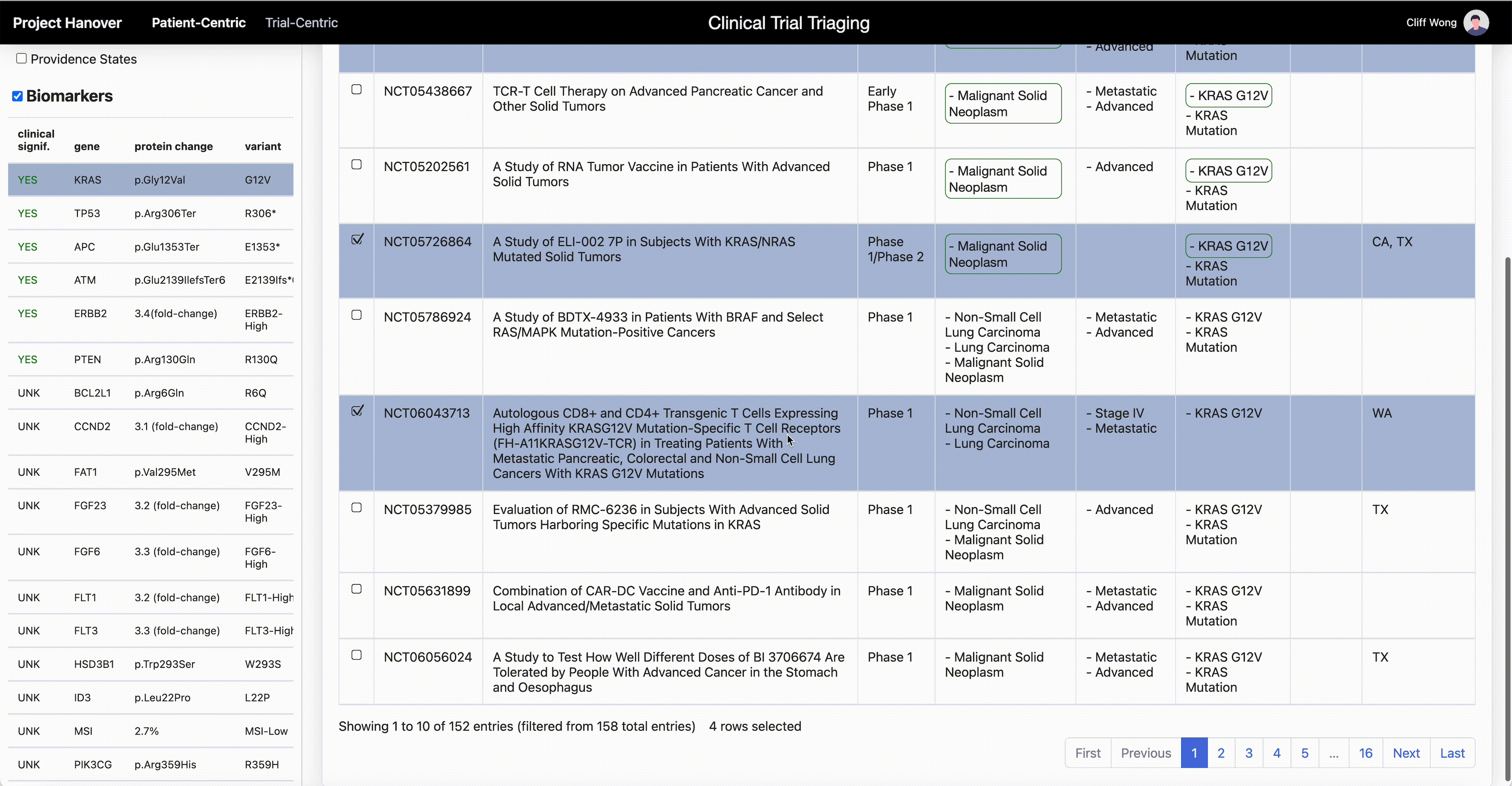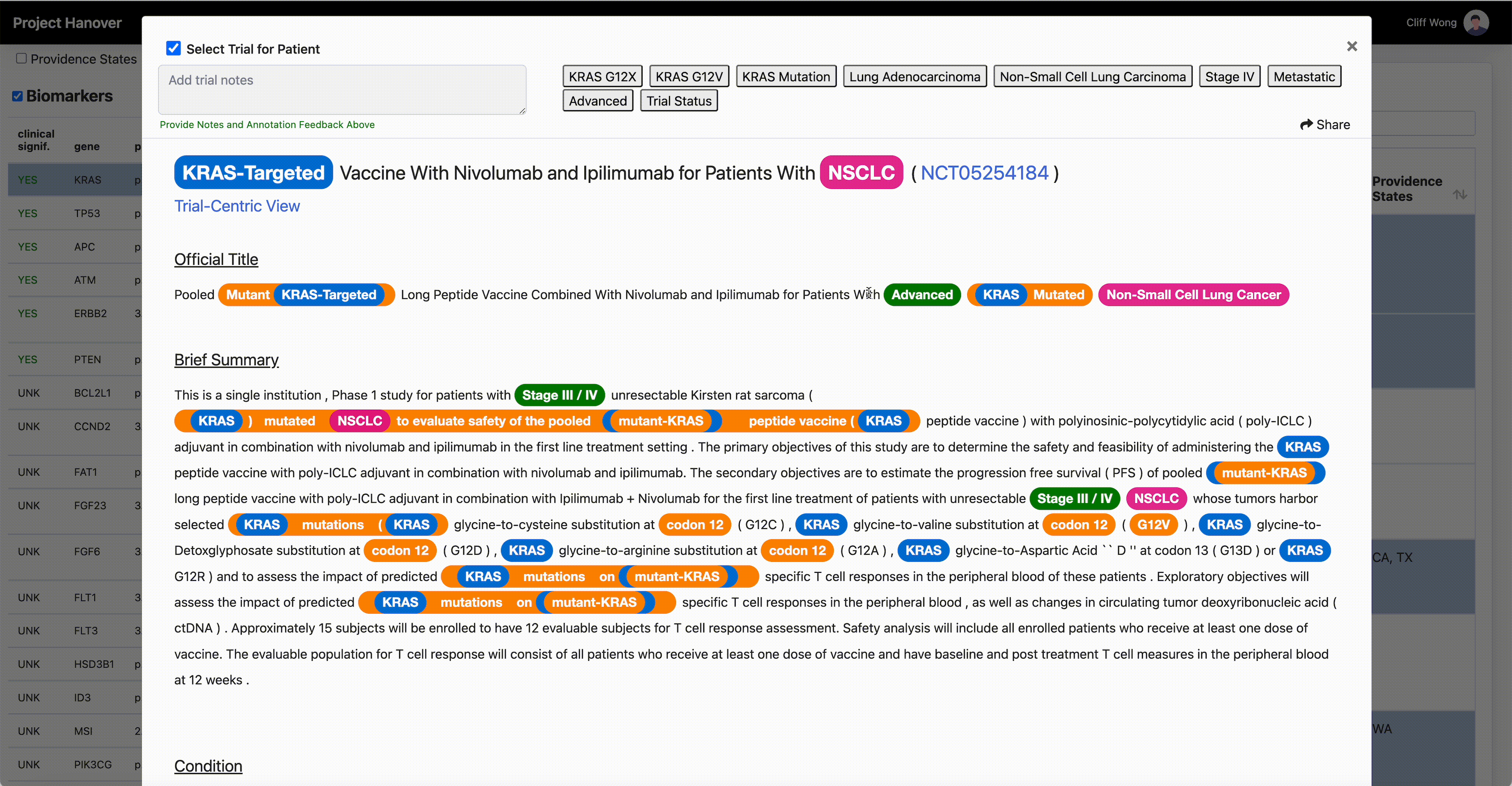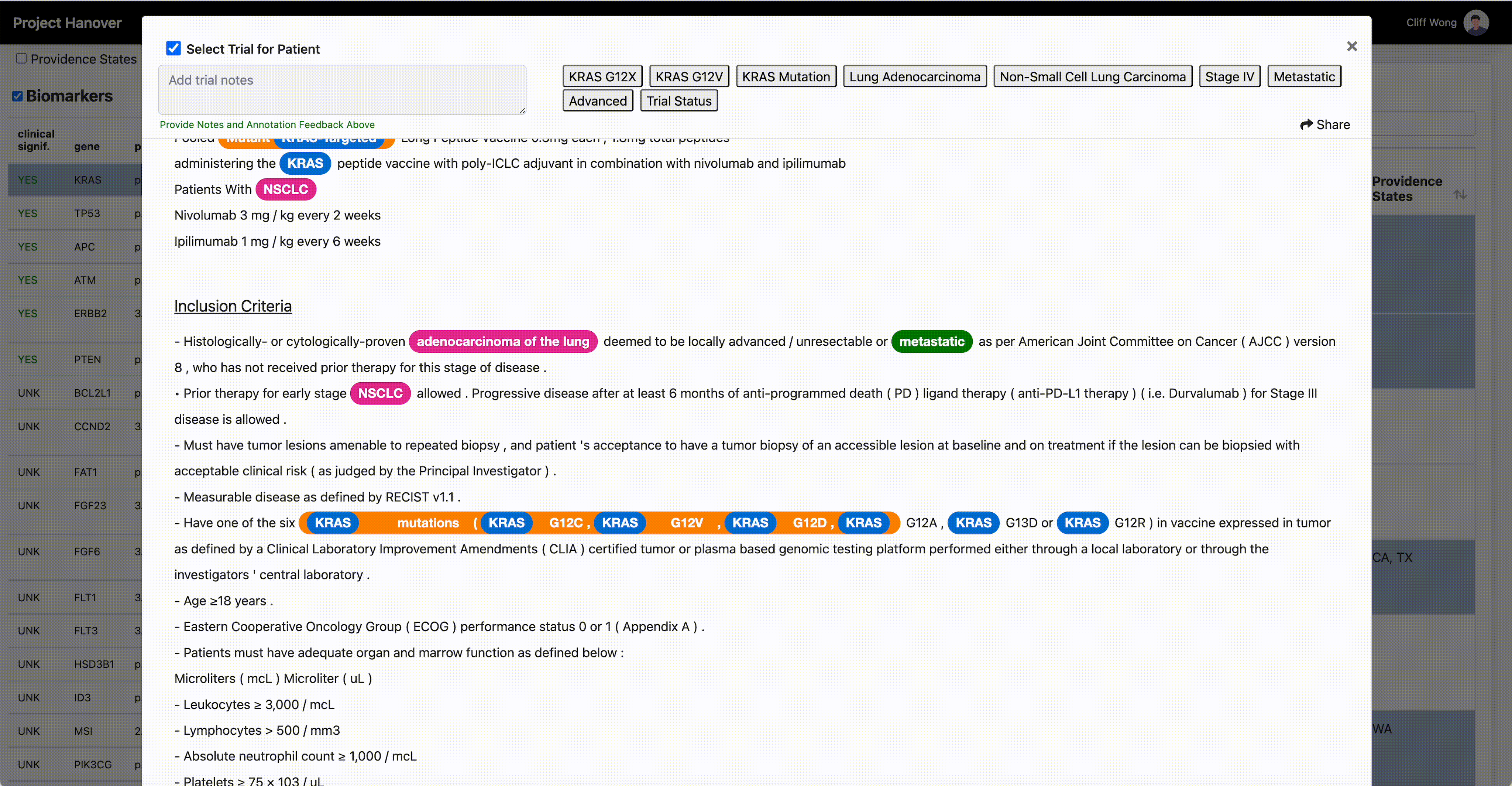
Esta demostración muestra cómo la herramienta de IA ayuda a los médicos a analizar de manera eficiente los criterios de los ensayos clínicos de un paciente. (Cortesía de Providence)
El progreso es notable en varios niveles. Las máquinas de diagnóstico que generan cantidades tan grandes de datos no existían hace un par de años. La IA también ha mejorado en ese tiempo: el equipo de investigación conjunto de Providence y Microsoft explora la vanguardia de los modelos básicos y va más allá para cerrar la brecha de competencia en la salud de precisión. La oncología puede ser la punta de lanza, pero la expansión exponencial de los flujos de datos, que convergen en cada visita al consultorio del médico, con el tiempo, impactará en todas las áreas de la medicina.
Los prototipos de IA de Providence se entrenaron con estos datos holísticos y multimodales de los pacientes. Microsoft ayudó a Providence a procesar imágenes radiológicas heredadas: más de dos millones de estudios con 600 millones de imágenes. Todo el cómputo se llevó a cabo dentro del inquilino privado de Providence y fue aprobado por la Junta de Revisión Institucional (IRB, por sus siglas en inglés) de Providence, adhiriéndose a los estándares apropiados de privacidad y cumplimiento.1
Microsoft también ayudó a Providence a digitalizar todas las diapositivas de patología del cáncer (más de 100 mil imágenes de diapositivas completas) como imágenes de ultra alta resolución para convertirlas en otro conjunto de entrenamiento de IA de investigación. Desde entonces, el equipo conjunto ha logrado grandes avances en el entrenamiento previo de potentes modelos biomédicos multimodales (LMM, por sus siglas en inglés) a partir de datos del mundo real, multimodales y a gran escala.
«La integración multimodal del paciente resultante puede servir como un gemelo digital para el paciente y permitir el razonamiento similar al del paciente a escala», dice Poon. «Esta evidencia del mundo real a nivel poblacional puede mejorar la atención al paciente al identificar lo que funciona y acelerar el descubrimiento biomédico al identificar dónde y cómo no funciona».
Todavía faltan muchas piezas del rompecabezas, o píxeles que aumentarían la resolución de la imagen, o existen como datos que no se están analizando.
«Todas las otras cosas que todavía no capturamos, influyen e impactan en los resultados del paciente», dice el Dr. Bifulco. «En la actualidad, en el entorno experimental, estás limitado por los aspectos computacionales. La IA puede desempeñar un papel importante».
1Protocolos #2019000204 y 2019000206 del IRB de Providence.
Foto de portada: Las pruebas médicas más complejas generan enormes cantidades de datos. La IA ayuda a analizar esos datos mucho más rápido, y el tiempo es esencial para los pacientes con cáncer. (Foto de sinology/Getty Images)

